Fisioter Bras 2022;2395):760-73
REVISÃO
A eficácia da terapia de
movimento induzido por contensão em crianças menores de 3 anos: uma revisão
sistemática
The efficacy of restraint-induced movement therapy in children under 3 years
of age: a systematic review
Gabriela de Souza
Rodrigues*, Elkmara Gabriela Ferreira*, Caroline
Pires Teixeira*, Deisiane Oliveira Souto**
*Faculdade de Santa Luzia
(UNIESP), **Faculdade de Santa Luzia (UNIESP), Universidade Federal de Minas
Gerais (UFMG)
Recebido em 15 de fevereiro
de 2022; Aceito em 7 de julho de 2022.
Correspondência: Deisiane
Oliveira Souto, Programa de Pós-Graduação em Ciências da Reabilitação
Departamento de Fisioterapia, Escola de Educação Física, Fisioterapia e Terapia
Ocupacional, Universidade Federal de Minas Gerais, Avenida Antônio Carlos, 6627
Belo Horizonte MG
Gabriela
de Souza Rodrigues: gabriela.s2808@gmail.com
Elkmara Gabriela Ferreira:
elkmaragabriela1@gmail.com
Caroline
Pires Teixeira: carolline566@gmail.com
Deisiane Oliveira Souto:
deisiane.souto@gmail.com
Resumo
Introdução: A terapia de movimento induzido por
contensão (TMIC) é a abordagem de tratamento mais utilizada na reabilitação do
membro superior de crianças com Paralisia Cerebral Unilateral (PCU) e Paralisia
Braquial Perinatal (PBP). Protocolos adaptados da TMIC (Baby-TMIC) têm sido
utilizados em crianças menores que três anos, porém seus benefícios não são
totalmente conhecidos. Objetivo: Avaliar a eficácia da Baby-TMIC na
reabilitação do membro superior de crianças com comprometimentos unilaterais
menores que 3 anos de idade. Métodos: Trata-se de uma revisão
sistemática. A busca e a seleção dos estudos foram realizadas por dois
investigadores independentes durante o período de maio de 2021, nas bases Pubmed, Embase, PEDro, Lilacs e Scielo. A escala PEDro foi utilizada para avaliar a qualidade metodológica
dos estudos. A qualidade geral das evidências e a força das recomendações foram
avaliadas pela GRADE. Resultados: Cinco estudos foram incluídos e
incorporaram um total de 190 crianças, com idade variando de 6 a 30 meses.
Quatro estudos envolveram crianças com PCU e apenas um estudo envolveu crianças
com PBP. Os escores da escala PEDro variaram de 5 a
7, com média 5,8 pontos. A Baby-TMIC resultou em melhorias no desempenho
bimanual, unimanual, função motora grossa, atividades
de vida diária e movimentação ativa. A qualidade da evidência variou de baixa a
muito baixa. Conclusão: Esta revisão fornece as evidências mais
atualizadas sobre a eficácia da Baby-TMIC na reabilitação do membro superior de
crianças com PCU e PBP menores de 3 anos.
Palavras-chave: paralisia cerebral; paralisia braquial
perinatal; terapia de movimento induzida por contensão; crianças.
Abstract
Introduction: Constraint-induced movement therapy (CIMT) is the
most commonly used treatment approach in upper limb rehabilitation of children
with Unilateral Cerebral Palsy (UCP) e Perinatal Brachial Palsy (PBP). Adapted
CIMT protocols (Baby- CIMT) have been used in children younger than three years
of age, however, their benefits are not fully known. Objective: To
evaluate the efficacy of Baby-CIMT in the rehabilitation of the upper limb of
children with unilateral impairments younger than 3 years of age. Methods:
This is a systematic review. The search and selection of studies were carried
out by two independent investigators during the period of May 2021, in the
following electronic databases: Pubmed, Embase, PEDro, Lilacs and Scielo. The PEDro scale was used to assess the methodological quality
of the studies. The overall quality of the evidence and the strength of the
recommendations were assessed by GRADE. Results: Five studies were
included and incorporated a total of 190 children, ranging in age from 6 to 30
months. Four studies involved children with UCP and only one study involved
children with PBP. The PEDro scale scores ranged from
5 to 7, with a mean of 5.8 points. Baby-CIMT resulted in improvements in
bimanual and unimanual performance, gross motor function, activities of daily
living and active movement. The quality of the evidence ranged from low to very
low. Conclusion: This review provides the most up-to-date evidence on
the effectiveness of Baby-CIMT in the rehabilitation of the upper limb of
children with UCP and PBP under 3 years of age.
Keywords: cerebral palsy; perinatal brachial palsy;
constraint-induced movement therapy; children.
Introdução
A
Paralisia Cerebral Unilateral (PCU) e a Paralisia Braquial Perinatal (PBP) são
condições que afetam crianças, resultando em redução no uso do membro afetado,
além de disfunção motora e postural [1,2,3]. A PCU é caracterizada por um
distúrbio sensório-motor unilateral, devido a distúrbios não progressivos que
ocorrem no cérebro fetal ou infantil [4,5]. A PBP consiste em uma lesão
neonatal que ocorre devido a uma complicação do parto, é caracterizada por uma
ou mais obstruções na condução nervosa no plexo braquial [6,7]. Ambas as
condições, PCU e PBP, evoluem com dificuldade na utilização do membro superior
acometido devido às alterações de força e amplitude de movimento, desenvolvendo
o “não uso aprendido” [8,9]. Estes déficits interferem no uso do membro
superior, bem como no desempenho bimanual, podendo resultar em limitações de
atividades simples, tais como vestir e tirar as roupas, amarrar cadarços ou
colocar os sapatos, escovar os dentes, abrir o pote de biscoitos, dentre outras
[10,11,12].
Na
maioria das vezes, as técnicas de reabilitação são introduzidas mais
tardiamente, não favorecendo os mecanismos plásticos alcançados com a
intervenção precoce [13]. A intervenção precoce é um conjunto de ações
multidisciplinares oferecidas a crianças com idade inferior a 5 anos que
apresentam riscos para o desenvolvimento infantil [14,15]. Visa estimular as
capacidades da criança o mais cedo possível, bem como apoiar a família e
oferecer um acompanhamento de forma preventiva ou minimizar os problemas
relacionados ao desenvolvimento neuropsicomotor [16,17]. Intervenções
fornecidas precocemente podem favorecer melhores resultados, devido à
neuroplasticidade, especialmente pela grande atividade cerebral e pelo
amadurecimento constante do sistema nervoso [18,19]. Atualmente, poucas
modalidades de intervenção precoce estão disponíveis para crianças com
comprometimentos unilaterais [20]. Dentre as técnicas existentes, destacam-se a
Terapia de Movimento Induzido por Contensão (TMIC) adaptada para bebês,
conhecida como Baby-TMIC [21].
A TMIC é
uma técnica usada em crianças com PCU e PBP, caracteriza-se pela restrição do
membro superior afetado associado ao treinamento intensivo do membro superior
acometido, objetivando “forçar” o uso do membro [22,23]. Além disso, fazem
parte do protocolo da TMIC métodos comportamentais que ajudam a aumentar a
adesão da criança ao tratamento [24,25]. O protocolo original da TMIC propõe 6
horas diárias de terapia, porém protocolos adaptados com intensidades mais
baixas foram desenvolvidos para aumentar a adesão das crianças [26].
Inicialmente a TMIC foi proposta para crianças maiores, mas tendo em vista a
importância da intervenção precoce, protocolos adaptados começaram a ser
utilizados em crianças menores de três anos (Baby-TMIC) [8,18,20,27]. A Baby-TMIC
é uma modificação da TMIC, adaptada para bebês e crianças com idade inferior a
18 meses com deficiência unilateral. A Baby-CIMT tem sido utilizada com duração
de 30 minutos por dia, 6 dias por semana, durante 12 semanas, apresentando
resultados significativos na melhora das atividades manuais e no
desenvolvimento precoce [20,21].
Apesar da
Baby-CIMT ter apresentado resultados promissores, a literatura não dispõe de
revisões sistemáticas que avalie seus benefícios em crianças com PCU e PBP. Diante
do exposto, o objetivo deste estudo é realizar uma revisão sistemática da
literatura a fim de verificar a eficácia da Baby-CIMT na reabilitação do membro
superior de crianças com PCU e PBP com idades inferiores a três anos.
Métodos
Uma
revisão sistemática foi realizada seguindo a declaração Preferred
Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA) [28]. O protocolo metodológico desta
revisão sistemática foi registrado no PROSPERO International
Prospective Register of Systematic Reviews (344631).
Procedimentos
Trata-se
de uma revisão sistemática da literatura. A procura de artigos foi realizada
por meio de uma busca computadorizada, durante o período de abril 2021, nas
bases de dados Pubmed, Embase, PEDro
Lilacs e Scielo. A
estratégia de busca incluiu termos que descreve a população alvo (paralisia
cerebral unilateral; paralisia braquial perinatal) e termos para o tipo de
intervenção (terapia do movimento induzido por contensão modificada; CIMT; CIMT
modificada; treinamento unilateral). As mesmas palavras foram utilizadas em
inglês. De acordo com cada banco de dados, foi utilizada uma combinação
específica de palavras-chave com os termos apropriados e os operadores and/or. A pesquisa secundária incluiu a verificação da
lista de referências dos artigos incluídos. A busca nas bases de dados foi
realizada por dois pesquisadores (EGF e GSR), de forma independente, e seguindo
os critérios de inclusão e exclusão estabelecidos abaixo. A primeira etapa de
seleção foi realizada através da leitura dos títulos e resumos de todos os
artigos. Após essa etapa, foi realizada a leitura na íntegra dos artigos
selecionados. Divergências entre os dois pesquisadores foram resolvidas por um
terceiro (CPT).
Critérios de inclusão e
exclusão
Foram
incluídos artigos completos envolvendo Baby-TMIC em comparação a fisioterapia
convencional ou outras intervenções; estudos envolvendo bebês ou crianças com
PCU ou PBP do nascimento até os 3 anos de idade; sem restrição de data,
publicados nos idiomas inglês ou português. Foram
excluídos todos os estudos divergentes do tema. Os artigos foram excluídos se
não tivessem um grupo de comparação que recebesse outras terapias ou
intervenções mínimas; estudos envolvendo participantes com outras condições
médicas diagnosticadas ou se não relataram dados de indivíduos com PCU e PBP
separadamente; estudos que não forneceram dados suficientes para inclusão na
síntese qualitativa desta revisão.
Extração dos dados
Dois
autores (EGF e GSR) extraíram e compilaram independentemente os dados de cada
artigo usando uma tabela no Microsoft Excel. Divergências entre os dois
pesquisadores foram resolvidas por um terceiro (CPT). As seguintes informações
foram extraídas dos estudos: tamanho amostral, características dos
participantes (faixa etária, sexo), características dos protocolos de
intervenção e intervenções controles, medidas de desfechos e principais
resultados referentes ao membro superior acometido após tratamento com a
Baby-CIMT.
Qualidade metodológica
A
qualidade metodológica dos estudos incluídos foi avaliada pela escala PEDro, descrita na base de dados PhysiotherapyEvidencDatabase
(www.pedro.org.au) [29]. A escala PEDro baseia-se em
uma lista composta por 11 itens, e foi desenvolvida para classificar e
qualificar as informações reportadas em cada estudo. Cada item contido na
tabela representa um ponto que, na soma total, varia de zero a 10 pontos
(primeiro item não é pontuado). Os escores da PEDro
dos estudos foram categorizados como alto risco de viés (3 de 10 pontos), risco
moderado (de 4 a 5 de 10 pontos) ou baixo risco de viés (6 de 10 pontos ou
mais) [30].
Qualidade da evidência
A
qualidade geral das evidências e a força das recomendações foram avaliadas
utilizando-se o sistema de Avaliação, Desenvolvimento e Avaliação da
Classificação de Recomendações – GRADE [31]. Este sistema especifica quatro
níveis evidência: alto (evidência suficiente na estimativa do efeito), moderado
(o efeito verdadeiro está próximo da estimativa do efeito), baixo (a confiança
do efeito é limitada) e muito baixo (pouca confiança da estimativa do efeito).
A evidência geral foi rebaixada dependendo da presença de cinco fatores: 1)
risco de viés; 2) inconsistência dos resultados; 3) indireto; 4) imprecisão e
5) viés de publicação. Os critérios GRADE foram avaliados pelo consenso de dois
examinadores, seguindo as diretrizes relatadas [32].
Resultados
A
estratégia de pesquisa nas bases de dados identificou 919 estudos
potencialmente relevantes. Após a triagem por título e resumo, 35 registros
atenderam aos critérios iniciais e foram revisados de forma independente para
inclusão. Destes, cinco estudos foram elegíveis e incluídos na revisão para
análise posterior [8,12,18,20,27]. A Figura 1 mostra o fluxograma com o
processo de seleção dos estudos.
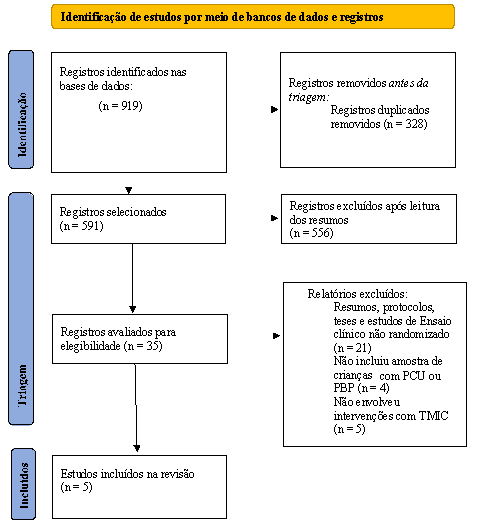
Figura 1 - Diagrama de fluxo do estudo
Os
artigos selecionados foram sumariados na tabela I. Dos cinco estudos incluídos
na revisão, quatro são ensaios clínicos randomizados [8,18,20,27] e um estudo é
retrospectivo [18]. A amostra total foi de 190 participantes, com idade
variando de 6 a 30 meses. Todos os estudos incluíram bebês com deficiência
unilateral, quatro estudos [8,18,20,27] envolveram crianças com PCU e apenas um
estudo [12] envolveu crianças com PBP. Todos os estudos utilizaram programas de
treinamento envolvendo Baby-TMIC como forma de intervenção. A intervenção foi
em média de 6,6 semanas, sendo a duração mínima de 3 semanas [8] e duração
máxima de 12 semanas [20], com frequência média de 5,8 dias por semana. No que
se refere à terapia controle, três estudos [8,12,18] utilizaram a fisioterapia
convencional, um estudo [20] utilizou massagem para bebês e um estudo [27]
utilizou o treinamento intensivo bimanual.
No que se
refere aos instrumentos de medida utilizados nos estudos para avaliação da
efetividade da intervenção, o Assisting Hand
Assessment (AHA), que avalia o desempenho bimanual da mão, foi a medida mais
empregada, sendo utilizada em três estudos [18,20,27]. Um dos estudos [20]
utilizou o Hand Assessment for Infants (HAI), que
avalia o desempenho unimanual da mão. Outro [8]
utilizou o Pediatric Evaluation
of Disability Inventory (PEDI) e o Pediatric
Motor Activity Log (PMAL), que avaliam as atividades
de vida diária, e o Gross Motor Function Measure (GMFM) na avaliação da função motora grossa. Estudo
[27] utilizou o Functional Inventory
(FI) na avaliação da função motora grossa e função da mão e o Mini-Assisting Hand Assessment (Mini-AHA)
que avalia o uso bimanual das mãos. Outro estudo [12] utilizou o Active Motion Scale (MAS), que avalia o movimento ativo do membro
superior.
Tabela I - Características dos estudos e principais
resultados
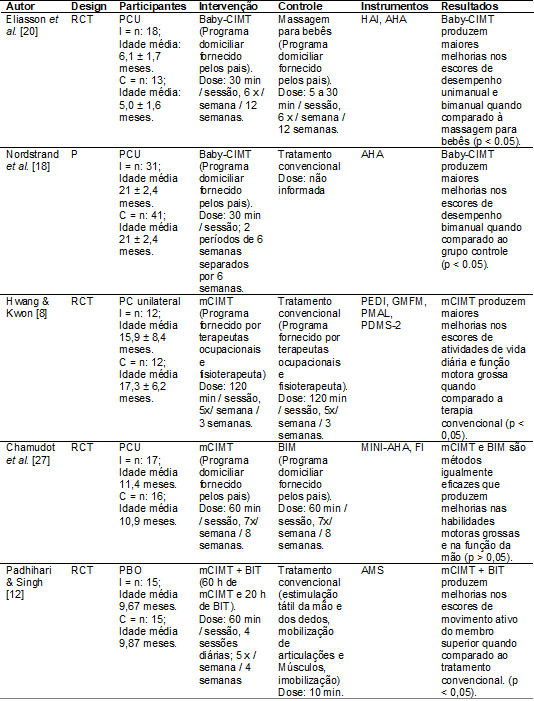
I = intervenção; C = controles; P = prospectivo; RCT =
Randomized Clinical Trial; CIMT = constraint-induced movement therapy; mCIMT = modified constraint-induced movement therapy; PCU =
Paralisia Cerebral Unilateral; AHA = Assisting Hand
Assessment; HAI = Hand Assessment for Infants; GMFM = Gross Motor Function
Measurement; PEDI = Pediatric Assessment of Disability Inventory; BIM =
bimanual therapy; FI = Functional Inventory; Mini AHA = Mini Assisting Hand
Assessment; BIT = Bimanual Intensive Therapy; MAS = Active movement scale;
PDMS-2 = Peabody Developmental Motor Scales-2; PMAL = Pediatric Motor Activity
Log
A
qualidade metodológica dos estudos, conforme a escala PEDro,
variou de 5 a 7, com média 5,8 pontos (tabela II). Nenhum dos estudos
apresentou sujeitos cegos e terapeutas cegos. Todos os estudos pontuaram os
itens “acompanhamento adequado”, “comparações entre grupos” e “estimativas
pontuais e variabilidade”. Sessenta por cento (60%) dos estudos apresentaram
baixo risco de viés, enquanto 40% dos estudos apresentaram risco moderado.
Nenhum estudo apresentou alto risco de viés. Dois estudos [8,27] tiveram suas
pontuações retiradas do site PEDro. Três estudos
[12,18,20] não tiveram suas pontuações disponíveis no site e, portanto, foram
pontuados por dois pesquisadores diferentes (EGF e GSR), com discordâncias
resolvidas por um terceiro pesquisador (CPT).
Tabela II – Qualidade metodológica dos estudos
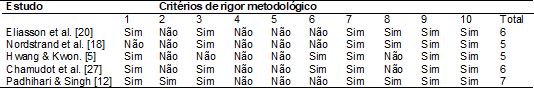
1
=
Critério de eleição; 2 = Alocação
aleatória; 3 = Alocação oculta; 4 =
Comparabilidade
de linha de base; 5 = Assuntos cegos; 6 = Terapeutas cegos; 7 =
Avaliadores
cegos; 8 = Acompanhamento adequado; 9 = Análise de
intenção de tratar; 10 =
Comparações entre grupos; 11 = Estimativas pontuais e
variabilidade
Em
relação aos resultados relacionados à eficácia da Baby-TMIC, três estudos
[8,12,20] encontraram melhoras significativas no grupo intervenção, quando
comparado ao grupo controle. Apenas um estudo [27] não encontrou diferenças
estatísticas entre os grupos intervenção e controle. Três estudos [18,20,27]
encontraram melhora no desempenho bimanual. Dois estudos [8,27] encontraram
melhora na função motora grossa. Dois estudos [20,27] encontraram melhora do
uso unimanual. O nível de evidência para essas
comparações foi classificado como muito baixo. Um estudo [8] encontrou melhora
nas atividades de vida diária tais como, autocuidado, mobilidade e função
social; um estudo [12] mostrou melhora no movimento ativo do membro superior.
Para esses desfechos, o nível de evidência foi classificado como baixo.
Discussão
A
presente revisão teve como objetivo avaliar a efetividade da Baby-TMIC na
reabilitação do membro superior de crianças com comprometimentos unilaterais
menores que 3 anos de idade, como na PCU e PBP. De forma geral, a Baby-TMIC se
mostrou uma intervenção eficaz. Dos cinco estudos [8,12,18,20,27] incluídos na
revisão, quatro [8,12,18,20] encontraram melhora significativa no grupo
intervenção quando comparado ao grupo controle. Apenas um estudo [27] não
encontrou diferenças estatísticas, a Baby-TMIC se mostrou igualmente eficaz ao
treinamento intensivo bimanual.
Embora a
média de tempo de duração da intervenção foi de 1 hora, houve uma variabilidade
entre os estudos. Dois estudos [18,20] utilizaram um protocolo de 30 min e dois
estudos [12,27] utilizaram um protocolo de 1 hora. Apenas um estudo [8]
utilizou protocolo com duração de duas horas. A literatura tem sugerido
protocolos de 30 minutos por se tratar de bebês, uma vez que eles podem não
tolerar tempos maiores. Protocolos com tempos maiores podem ser cansativos para
bebês e suas famílias. Além disso, existem evidências de que 30 min são
suficientes para gerar mudanças plásticas no sistema nervoso central da criança
e que essas mudanças resultam em ganhos motores e funcionais do membro superior
acometido [20,21].
Diferentes
instrumentos foram utilizados na avaliação da efetividade da Baby-TMIC em
crianças com PCU e PBP. Há uma dificuldade em encontrar instrumentos que
avaliem especificadamente o membro superior em crianças com PCU e PBP com
idades inferiores a três anos. Atualmente o mais apropriado para esse fim é o
HAI, que foi adaptado a partir do AHA. Em populações maiores, o AHA é um
instrumento amplamente utilizado para avaliar crianças com deficiência
unilateral. Outros instrumentos usados pelos estudos incluídos na revisão são:
GMFM, PDMS e GMS utilizados na avaliação das funções motoras grossas; o PEDI e
o PMAL para mensuração das atividades de vida diária e o AMS para avaliação do
movimento ativo de membro superior. Embora todos esses instrumentos sejam
padronizados e válidos, não são específicos para avaliação de deficiências
unilaterais.
Utilizando
os critérios estabelecidos na GRADE [32], a qualidade da evidência foi
classificada entre baixa e muito baixa qualidade. Em geral, os estudos foram
rebaixados devido ao alto risco de viés (incluindo falta de cegamento devido à
impossibilidade de cegar os participantes) e imprecisão (número pequeno de
participantes). Além disso, a qualidade metodológica dos estudos, em média, foi
de 5,8, o que indica risco moderado de viés. Dessa forma, é possível que
evidências robustas alterem as estimativas dos efeitos dessa intervenção.
Esta
revisão apresenta algumas limitações para a generalização e interpretação dos
resultados. A heterogeneidade dos desfechos e dos instrumentos de medida
utilizados nos estudos impossibilitou a realização de meta-análise. A
generalização dos resultados é limitada para a população de crianças com PBO,
já que apenas um estudo incluiu participantes com essa condição de saúde. Um
pequeno número de estudos foi incluído, com tamanhos de amostras pequenos, o
que reduz a acurácia dos achados. Além disso, nem todos são ensaios clínicos
randomizados. Por fim, os desfechos avaliados nos estudos foram bastante
diversificados, o que dificulta conclusões definitivas sobre a eficácia da
Baby-TMIC.
Conclusão
O
objetivo da presente revisão foi avaliar a eficácia da Baby-TMIC na
reabilitação de crianças com comprometimentos unilaterais com idades inferiores
a três anos. Existem evidências de muito baixa qualidade de que a Baby-TMIC é
mais eficaz do que outras intervenções na melhora do desempenho bimanual,
desempenho unimanual e função motora grossa. Além
disso, evidências de baixa qualidade mostraram superioridade da baby-TMIC na
melhora das atividades de vida diária e movimento ativo de membro superior quando
comparado a outras intervenções. Considerando o pequeno número de estudos
disponíveis, bem como o pequeno tamanho amostral dos mesmos, novos estudos
ainda são necessários.
Conflitos
de interesse
Os autores
declaram não haver conflito de interesses
Fontes
de financiamento
O presente
estudo foi financiado pelo Conselho Nacional de Desenvolvimento Científico e
Tecnológico - CNPq (bolsa nº 150010/2022-2).
Contribuição
dos autores
Concepção
e desenho da pesquisa:
Souto DO, Rodrigues GS, Ferreira EG, Teixeira CP; Pesquisa nas bases de
dados: Rodrigues GS, Ferreira EG, Teixeira CP; Seleção dos estudos:
Rodrigues GS, Ferreira EG, Teixeira CP; Análise e interpretação dos dados:
Souto DO, Rodrigues GS, Ferreira EG, Teixeira CP; Redação do manuscrito:
Souto DO, Rodrigues GS, Ferreira EG, Teixeira CP; Revisão crítica do
manuscrito quanto ao conteúdo intelectual importante: Souto DO, Rodrigues
GS, Ferreira EG, Teixeira CP
Referências
- Eren B, Saygı
EK, Tokgöz D, Leblebicier
MA. Modified constraint-induced movement therapy during hospitalization in
children with perinatal brachial plexus palsy: A randomized controlled trial. J
Hand Ther 2020;33(3):418-25. doi: 10.1016/j.jht.2019.12.008 [Crossref]
- Novak I, Morgan C, Adde L, Blackman J, Boyd RN, Brunstrom-Hernandez J, et al. Early, accurate diagnosis and early intervention in cerebral palsy: advances in diagnosis and treatment. JAMA Pediatr 2017;171(9):897-907. doi: 10.1001/jamapediatrics.2017.1689 [Crossref]
- Holmström LIN, Vollmer B, Tedroff K, Islam M, Persson JK, Kits A, et al. Hand function in relation to brain lesions and corticomotor-projection pattern in children with unilateral cerebral palsy. Dev Med Child Neurol 2010;52(2):145-52. doi: 10.1111/j.1469-8749.2009.03496.x [Crossref]
- Gordon AM. To constrain or not to constrain, and other stories of intensive upper extremity training for children with unilateral cerebral palsy. Dev Med Child Neurol 2011;53:56-61. doi: 10.1111/j.1469-8749.2011.04066.x [Crossref]
- Morgan C, Darrah J, Gordon AM, Harbourne R, Spittle A, Johnson R, Fetters L. Effectiveness of motor interventions in infants with cerebral palsy: a systematic review. Dev Med Child Neurol 2016;58(9):900-9. doi: 10.1111/dmcn.13105 [Crossref]
- Lopes AR, Alves CAL, Campos
PDBF, Silva RMP, Santos CCT. Atuação fisioterapêutica na paralisia braquial
obstétrica. Revista de Iniciação Científica e Extensão [Internet] 2020 [cited 2022 Aug 31];3(2):412-19. Available from:
https://revistasfacesa.senaaires.com.br/index.php/iniciacao-cientifica/article/view/305
- Andersen J, Watt J, Olson J, & Van Aerde J. Perinatal brachial plexus palsy. Paediatr Child Health 2006;11(2):93-100. doi: 10.1093/pch/11.2.93 [Crossref]
- Hwang YS, Kwon JY. Effects of modified constraint-induced movement therapy in realworld arm use in young children with unilateral cerebral palsy: a single-blind randomized trial. Neuropediatrics 2020;51(4):259-66. doi: 10.1055/s-0040-1702220 [Crossref]
- Dodds SD, Wolfe SW. Perinatal brachial plexus palsy. Current Opinion in Pediatrics 2000;12(1):40-7. doi: 10.1097/00008480-200002000-00009 [Crossref]
- Medeiros DLD, Agostinho NB, Mochizuki L, Oliveira ASD. Quality of life and upper limb function of children with neonatal brachial plexus palsy. Rev Paul Pediatr 2020;38. doi: 10.1590/1984-0462/2020/38/2018304 [Crossref]
- Palmer FB. Strategies for the early diagnosis of cerebral palsy. J Pediatr 2004;145(2):S8-S11. doi: 10.1016/j.jpeds.2004.05.016 [Crossref]
- Padhihari S, Singh P. Effectiveness of modified constraint induced movement therapy-bimanual intensive therapy in improving upper extremity function in children with obstetric brachial plexus injury. Indian J Occup Ther 2017;49(3):91-6. doi: 10.5014/ajot.2018.025981 [Crossref]
- Santos GFL. Atuação da
fisioterapia na estimulação precoce em criança com paralisia cerebral. DêCiência em Foco
[Internet]. 2018 [cited 2022 Aug 30];1(2). Available from:
https://revistas.uninorteac.com.br/index.php/DeCienciaemFoco0/article/view/76#
- Spittle A, Orton J, Anderson PJ, Boyd R, Doyle LW. Early developmental intervention programmes provided post hospital discharge to prevent motor and cognitive impairment in preterm infants. Cochrane Database of Systematic Reviews 2015;(11). doi: 10.1002/14651858.CD005495.pub4 [Crossref]
- Novak I, Morgan C, Adde L, Blackman J, Boyd RN, Brunstrom-Hernandez J, Badawi N. Early, accurate diagnosis and early intervention in cerebral palsy: advances in diagnosis and treatment. JAMA Pediatrics 2017;171(9):897-907. doi: 10.1001/jamapediatrics.2017.1689 [Crossref]
- Morgan C, Novak I, Dale RC, Guzzetta A, &
Badawi N. Single blind randomised controlled trial of
GAME (Goals Activity Motor Enrichment) in infants at high risk of cerebral
palsy. Res Dev Disabil 2016;55:256-67. doi: 10.1016/j.ridd.2016.04.005
- Hadders-Algra M. Early diagnosis and early intervention in cerebral palsy. Front Neurol 2014;5:185. doi: 10.3389/fneur.2014.00185 [Crossref]
- Nordstrand L, Holmefur M, Kits A, Eliasson AC. Improvements in bimanual hand function after baby-CIMT in two-year old children with unilateral cerebral palsy: A retrospective study. Res Dev Disabil 2015;41-2:86-93. doi: 10.1016/j.ridd.2015.05.003 [Crossref]
- Cioni G, D'Acunto G, Guzzetta A. Perinatal brain damage in children: neuroplasticity, early intervention, and molecular mechanisms of recovery. Prog Brain Res 2011;189:139-54. doi: 10.1016/B978-0-444-53884-0.00022-1 [Crossref]
- Eliasson AC, Nordstrand L, Ek L, Lennartsson F, Sjöstrand, L, Tedroff K, Krumlinde-Sundholm L. The effectiveness of Baby-CIMT in infants younger than 12 months with clinical signs of unilateral-cerebral palsy; an explorative study with randomized design. Res Dev Disabil 2018;72:191-201. doi: 10.1016/j.ridd.2017.11.006 [Crossref]
- Eliasson AC, Sjöstrand L, Ek L, Krumlinde-Sundholm L, Tedroff K. Efficacy of baby-CIMT: study protocol for a randomised controlled trial on infants below age 12 months, with clinical signs of unilateral CP. BMC Pediatr 2014;14(1):1-11. doi: 10.1186/1471-2431-14-141 [Crossref]
- Taub E, Crago JE, Uswatte
G. Constraint-induced movement therapy: A new approach to treatment in physical
rehabilitation. Rehabilitation Psychology 1998;43(2):152. doi: 10.1037/0090-5550.43.2.152 [Crossref]
- Eliasson AC, Krumlinde-Sundholm L, Shaw K, Wang C. Effects of constraint-induced movement therapy in young children with hemiplegic cerebral palsy: an adapted model. Dev Med Child Neurol 2005;47(4):266-75. doi: 10.1017/S0012162205000502 [Crossref]
- Grotta JC, Noser EA, Ro T, Boake C, Levin H, Aronowski J, Schallert T. Constraint-induced movement therapy. Stroke 2004;35:2699-701. doi: 10.1161/01.STR.0000143320.64953.c4 [Crossref]
- Morris DM, Taub E, Mark VW. Constraint-induced movement therapy:
characterizing the intervention protocol. Europa Medicophys
[Internet]. 2006 [cited 2022 Aug 30];42(3):257. Available from: https://pubmed.ncbi.nlm.nih.gov/17039224/
- Brito BM, Mancini MC, Vaz DV, Pereira de Melo AP, Fonseca ST. Adapted version of constraint-induced movement therapy promotes functioning in children with cerebral palsy: a randomized controlled trial. Clin Rehabil 2010;24(7):639-47. doi: 10.1177/0269215510367974 [Crossref]
- Chamudot R, Parush S, Rigbi A, Horovitz R, Gross-Tsur V. Effectiveness of modified constraint-induced movement therapy compared with bimanual therapy home programs for infants with hemiplegia: a randomized controlled trial. Am J Occup Ther 2018;72(6). doi: 10.5014/ajot.2018.025981 [Crossref]
- Liberati A, Altman DG, Tetzlaff J, Mulrow C, Gøtzsche PC, Ioannidis JP, et al. The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate health care interventions: explanation and elaboration. J Clin Epidemiol 2009;62:e1-e34. doi: 10.1016/j.jclinepi.2009.06.006 [Crossref]
- Maher CG, Sherrington C, Herbert RD, Moseley AM, Elkins M. Reliability of the PEDro scale for rating quality of randomized controlled trials. Phys Ther 2003;83:713-21. doi: 10.1093/ptj/83.8.713 [Crossref]
- Sherrington C, Herbert RD, Maher CG, Moseley AM. PEDro. A database of randomized trials and systematic reviews in physiotherapy. Man Ther 2000;5:223-6. doi: 10.1054/math.2000.0372 [Crossref]
- Schünemann H, Brożek J, Guyatt G, Oxman A. Handbook for grading the quality of evidence and the strength of recommendations using the GRADE approach. Updated October, 2013. doi: 10.1016/j.jclinepi.2013.02.003 [Crossref]
- Guyatt GH, Oxman AD, Kunz R, Woodcock J, Brozek J, Helfand M. GRADE Working Group. GRADE guidelines: 7. Rating the quality of evidence - inconsistency. J Clin Epidemiol 2011;64(12):1294-302. doi: 10.1016/j.jclinepi.2011.03.017 [Crossref]
